|
|
Presidęncia da República |
|
|
Presidęncia da República |
DECRETO No 68.603, DE 10 DE MAIO DE 1971.
|
Dispőe sôbre a execuçăo do Ajuste de Complementaçăo nş 15 sôbre produtos da Indústria Químico-Farmacęutica, concluído entre a Argentina, o Brasil e o México. |
O PRESIDENTE DA REPÚBLICA, usando das atribuiçőes que lhe confere o artigo 81, item III, da Constituiçăo, e
Considerando que o Tratado de Montevidéu aprovado pelo Decreto Legislativo de 3 de fevereiro de 1961, que criou a Associaçăo Latino-Americana de Livre Comércio, prevę, no seu artigo 16 a celebraçăo de Ajustes de Complementaçăo por setores industriais, matéria essa regulamentada pelas Resoluçőes 15 (I), 16 (I), e 99 (IV), da Confluęncia das Partes Contratantes do Tratado;
Considerando que os Plenipotenciários da Argentina, do Brasil e do México, com base nos dispositivos acima citados, assinaram, em Montevidéu, no dia 4 de dezembro de 1970, Protocolo estabelecendo um Ajuste de Complementaçăo sôbre produtos da Indústria Químico-Farmacęutica;
Considerando que, em cumprimento ao artigo 17 do Tratado de Montevidéu, e nos tęrmos do artigo 18 da Resoluçăo 99 (IV), o Comitę Executivo Permanente da ALALC, pela Resoluçăo 226 de 8 de janeiro de 1971, declarou as disposiçőes do presente Ajuste, que recebeu o número 15, compatíveis com os princípios do Tratado;
Considerando que o presente Ajuste deverá entrar em vigor sessenta dias após ter sido declarada sua compatibilidade, segundo dispőe o seu artigo 17;
decreta:
Art. 1ş A partir de 9 de março de 1971, as importaçőes dos produtos especificados no artigo 1ş do Protocolo anexo a ęste Decreto, originários da Argentina, do México e dos países considerados de menor desenvolvimento econômico relativo: Bolívia, Equador e Paraguai, ficam sujeitos aos gravames e requisitos específicos de origem estipulados no seu Anexo I, obedecidas as cláusulas e condiçőes estabelecidas no citado Protocolo.
Parágrafo único. As disposiçőes dęste Decreto năo se aplicam ŕs importaçőes provenientes dos países-membros da ALALC năo mencionadas neste artigo.
Art. 2ş O Ministério da Fazenda tomará, através dos órgăos competentes, as providęncias eventualmente necessárias ao cumprimento do disposto neste Decreto.
Art. 3ş A Comissăo Nacional para os Assuntos da ALALC, criada pelo Decreto nş 52.087, de 31 de maio de 1963 e reestruturada pelo Decreto nş 60.987, de 11 de julho de 1967, acompanhará, através da Carteira de Comércio Exterior do Banco do Brasil S.A., a execuçăo do Protocolo anexo, sugerindo as medidas julgadas necessárias ao seu fiel cumprimento.
Art. 4ş O presente Decreto entrará em vigor na data de sua publicaçăo, revogadas as disposiçőes em contrário.
Brasília, 10 de maio de 1971; 150ş da Independęncia e 83ş da República.
Emílio g. médici
Mário Gibson Barboza
Antônio Delfim Netto
Este texto năo substitui o publicado no DOU de 14.5.1971 e retificado em 18.5.1971.
PROTOCOLO DE AJUSTE DE COMPLEMENTAÇĂO SOBRE PRODUTOS DA INDÚSTRIA QUIMICO-FARMACĘUTICA
Os Plenipotenciários que subscrevem, devidamente autorizados por seus Governos e cujos poderes, achados em boa e devida forma, foram depositados na Secretaria do Comitę Executivo Permanente da Associaçăo Latino-Americana de Livre Comércio, convęm em celebrar um Ajuste de Complementaçăo no setor da indústria químico-farmacęutica, de conformidade com os Artigos 15, 16 e 17 do Tratado de Montevidéu e a Resoluçăo 99 (IV) da Conferęncia, o qual se regerá pelas disposiçőes do presente Protocolo.
CAPÍTULO I
Setor industrial
Art. 1ş O setor industrial abrangido pelo presente Ajuste compreende os produtos que se mencionam a seguir, com indicaçăo das respectivas posiçőes NABALALC.
NABALALC - PRODUTO
05.14.1.01 - Bile, inclusive dessecada (exceto extrato)
11.08.3.01 - Insulinas
12.07.0.03 - Cumaru (fava tonca, fava de sarrapia; sarapia) fresca ou sęca, inclusive cortada, triturada ou pulverizada
12.07.0.04 - Ipecacuanha (poaia) fresca ou sęca, inclusive cortada, triturada ou pulverizada
12.07.0.06 - Jalapa fresca ou sęca, inclusive cortada, triturada ou pulverizada
12.07.0.09 - Polígala fresca ou sęca, inclusive cortada triturada ou pulverizada
12.07.0.11 - Guaraná (uaraná) fresco ou sęco, inclusive cortado, triturado ou pulverizado
12.07.0.14 - Barbasco (cube) ou timbó fresco ou sęco, inclusive cortado, triturado ou pulverizado
13.03.1.01 - Suco e extrato de feto-macho
13.03.1.99 - Aloés; acônito folhas; acônito raiz; alcachôfra; anęmona, arnica; meimendro; beladona; benjoim; boldo; casca sagrada; castanha das índias (fruto); esporăo de centeio (ergonita, seundo Yvón ou segundo Bonjean); damiana; digital; drosera; estigmas de milho; frângula; galega; genciana; grindélia; funcho; hamamelis Virginia (casca); hamamelis Virginia (fôlhas); alface; liquen; lobélia; macela; simarruba; mirra; mostarda; nogal; noz de cola; noz vómica; oregăo; alcaçuz; passionária; passiflora incarnata; piscidia; polígala sęnega; quina vermelha; arruda; ruibarbo; salgueiro branco (casca); tilia; tolu; valeriana; viburno prunifólio
13.03.2.01 - Pactina cítrica
15.04.2.02 - Óleo de fígado de bacalhau refinado, para uso medicinal
15.08.9.99 - Mistura de azeite de girassol e oliveira, bromados, grau farmacęutico
28.15.0.99 - Sulfeto de selęnio micronizado
28.20.1.02 - Hidróxido de alumínio (alumínia hidratada) em pó, para uso farmacęutico
28.34.1.03 - Iodeto de potássio
28.34.1.04 - Iodeto de cálcio
28.34.2.02 - Iodeto de potássio
28.38.1.03 - Sulfato de bário, para uso farmacęutico
28.39.2.05 - Subnitrato de bismuto
28.42.1.08 - Carbonatos de bismuto (básico)
29.02.1.05 - Iodofórmio (triiodometano)
29.05.1.05 - Colasterol
29.05.1.10 - Metilandrostenediol (mestenediol; stendeiol; etc.)
29.05.1.11 - Alil-estrenol (17-alta-alilestr-4-en-17-beta-ol.; ou delta 4-17-alta-alil-17-beta-hidroxiestreno)
29.05.1.99 - Etinil-estrenol
29.05.1.99 - Etil-estrenol
29.06.2.03 - Hexilresorcinol (grau farmacęutico)
29.08.4.03 - Gliceril-guaiacol
29.08.4.04 - Gliceril-guetol
29.08.4.99 - Mefensina
29.08.5.02 - Sulfoguaiacolato de potássio
29.13.4.03 - Pregnenolona
29.13.4.99 - Epoxipregnenolona
29.13.4.99 - Dehidro-iso-androsterona
29.14.2.23 - Acetato de composto “S” de Reinchstein
29.14.2.99 - Monoacetato de pregnenolona
29.14.2.99 - Acetato de epoxipregnenolona
29.14.2.99 - Acetato de guaiacol
29.14.5.99 - Dipropionato de metilandrostenedio
29.14.7.04 - Benzoato de amônio
29.15.1.21 - Ácido succínico (grau farmacęutico)
29.15.1.99 - Fumarato de ferro (ferroso) para uso farmacęutico
29.16.2.01 - Ácido glocônico
29.16.2.02- Gluconato de cálcio
29.16.2.03 - Gluconato de sódio
29.16.2.04 - Gluconato de ferro para uso farmacęutivo
29.16.2.99 - Gluconogalacto-gluconato de cálcio
29.16.2.99 - Glucoheptonato de cálcio
29.16.2.99 - Bromolactobionato de cálcio
29.16.2.99 - Ácido cólico
29.16.2.99 - Ácido desoxicólico
29.16.2.99 - Desoxicolato de magnésio
29.16.2.99 - Desoxicolato de sódio
(1) 29.16.2.99 - Ácido biliar bruto total
(1) 29.16.2.99 - Sais biliares
29.16.2.99 - Ácido dehidrocólico
29.16.2.99 - Lactobionato de cálcio
29.16.2.99 - Gluconato de magnésio
29.16.2.99 - Dehidrocolato de Sódio
29.16.3.03 - Salicilato de Bismuto
29.16.3.12 - Galato básico de bismuto (subgalat)
29.16.3.99 - Florantirona ou ácido gama-exogama (8 fluoranteno) butílico (“zanchol”)
29.16.9.99 - Ácido pirúvico
29.16.9.99 - Ácido D-2 (6-metoxi 2,-naftil) propiônico (naproxen)
29.16.9.99 D-2-(6' metoxi-2'-naftil) propan-1.01
29.19.0.02 - Glicerofosfato de sódio
29.19.0.03 - Glicerofosfato de cálcio
29.19.0.99 - Inisotohexafosfato de cálcio e magnésio
29.19.0.99 - Glicerofosfato de magnésio
29.22.6.99 - Cloridrato de 5 - (3-dimetil amino propílideno) - (a, e) - dibenzocicloheptadieno
29.23.1.99 - Paranitrofenil-1-2-amino-propanodiol
29.23.1.99 - a-d-4 dimetilamino-1,2-difenil-3 metil-2-propionoxibutano (cloridato de dextropropxifeno)
29.23.1.99 - Napsilato de dextropopoxifeno
29.23.1.99 - Cloridrato de fenilefrina
29.23.4.99 - Ácido iodopanóico e seus sais
29.24.0.01 - Quelato de ferrocitrato de colina
29.25.1.99 - Mepromato
29.25.2.11 - Ácido 5-etil-5-isoamilbarbitúrico (amobarbitral)
29.25.2.11 - 5-etil-5-isoamilbarbiturato de sódio (amobarbital sódico)
29.25.2.11 - Ácido 5-alil-5- (1-metil-butil) - barbitúrico (secobarbital)
29.25.2.11 - 5-alil-5- (1-metil-butil) - barbiturato de sódio (secobarbital sódico)
29.25.2.11 - Ácido 0,5-dialil barbitúrico
29.25.2.11 - Ácido 5-etil-5- (1-metil-butil-barbitúrico)
29.25.2.11 - Pentobarbital (“embutal”) sódico
29.25.2.11 - Ácido 5-alil-5- (1-metil-propil)-barbitúrico
29.25.2.11 - Ácido 5-alil-5-isobutilbarbitúrico (butalbital)
29.25.2.93 - Acetilparafenetidina (fenacetina) grau farmacęutico
29.25.2.99 - Ácido acetrizóico (ácido 3-acetamido-2,4,6-triiodobenzóico)
29.25.2.99 - Metoclopramida ou monocloridrato de N-(diertilaminoetilo) -2 metoxi-4-amino-5-clorobenzamida
29.25.2.99 - Ácido diatrizóico
29.25.2.99 - Sal metil-gluatminico do ácido diatrizóico
29.25.2.99 - Sal sódico do ácido diatrizóico
29.25.3.99 - Dietilamina-2,6-acetoxilidina (xilocaína, lidocaína)
29.26.1.01 - Imidraortossulfobenzóica
29.26.2.99 - Cloridrato de 1,3 bis (clorobenzilidenamino) (“robenzinida”)
29.29.0.99 - Fenilsemicarbazida
29.29.0.99 - Oxima do acetato de pregnenolona
29.31.2.99 - Pentotal sódico ou tiopental sódio
29.31.6.06 - Metionina
29.31.6.99 - Acetil-D1-metionina para uso farmacęutico
29.31.6.99 - Acido tiazolidin-4-carboxílico
29.32.0.99 - Glicolilarsanilato de bismuto
29.32.0.99 - 3-nitro 4-hidroxifenil arsęnico
29.33.0.99 - Etilmercuriossalicilato de sódio
29.33.0.99 - Tiossalicilato de etilmercúrio
29.35.2.99 - Cloridrato de 1-metil-4- (5 deibenzo-(a, e) - ciclo heptatrienilideno) piperidina
29.35.2.99 - Hidrazia do ácido insonicotínico
29.35.2.99 - N-1-p. Tolueno sulfônico-4-ciano-fenil-piperidina (nitrilo-amida), uso farmacęutico
25.35.3.99 - 5-7-Diiodo-8-oxiquinoleína, 5-Cloro-7-iodo-8-oxiquinoleína, 5-7-Dicloro-8-oxiquinoleína
29.35.3.99 - 8-Hidroxiquinoleína
29.35.3.99 - 5,7-Diiodo-3-hidroxiquinoleína ou 5,7-Diiodoquinolinol (“searlequin”) ou diidoquin droga
29.35.3.99 - Dicloro-oxiquinoleína
29.35.3.99 - 5,7-dibromo-8-hidroxiquinoleína
29.35.5.01 - Piperazina (dietilendiamina)
29.35.5.99 - Dietilcarbamilmetilpiperazina
29.35.6.01 - Nucleinato de sódio
29.35.7.19 - Andrenolactona
29.35.7.99 - Espironolactona
29.35.7.99 - Glucono-delta-lactona
29.35.9.06 - Fenildimetilpirazolona
29.35.9.07 - Dimetilaminofenildimetilpirazolona
29.35.9.12 - Tiodifenilamina (fenotiazina)
29.35.9.12 - Tiodifenilamina (fenotiazina)
29.35.9.16 - Oximercuridibromofluoresceína dissódica
29.35.9.99 - Ácido xantogęnico
29.35.9.99 - Nitrofurano e furazolidona
29.35.9.99 - Nitrofurazona
29.35.9.99 - 1-(2-hidroxietil) -2-metil-5-nitroimidazol
29.35.9.99 - Brometo de propantelina (probantina) (meta-brometo beta-diisopropilamino-etil-9-xantenocarboxilato)
29.35.9.99 - 2-Carbetoxi-amiro-5-butil-benzimidazol
29.35.9.99 - Cloridato de difenoxilato ou cloridato de éster etílico do 2,2 difenil-4-(4-carboxifenilpiperidina)-butilonitrilo (lomotil)
29.35.9.99 - d1-2,3,5,6-tetraidro-6-fenilimidazo (2, 1-b) tiazol cloridrato (“tertamisole”)
29.36.0.01 - p-Aminobenzen-sulfamidotiazol (sulfatiazol)
29.36.0.02 - Sulfasuccinilsufatizol
29.36.0.03 - Sulfaftanilsulfatiazol
29.36.0.04 - Sulfaftalilacetamida
29.36.0.05 - Sulfaminotiazol
29.36.0.07 - p-aminobenzeno-sulfamidopirimidina (sulfadiazina)
29.36.0.08 - Cloropropramida
29.36.0.99 - n-(p-Acetil-fenil-sulfonil)-n-ciclo-hexil-uréia
29.38.1.01 - Carotenos (alfa, beta e gamma)
29.38.2.01 - Vitamina A-1
29.38.2.02 - Vitamina A-2
29.38.2.15 - Vitamina B-9 (ácidos fólicos)
29.38.2.19 - Pantotenato de cálcio
29.38.2.69 - 2-metil-3-fitil-1,4-naftoquinona (vitamina “K”)
29.38.2.71 - Nicotinamida
29.39.1.01 - Adrenocorticotropina (ACTH)
29.39.1.02 - Gonadotropinas
29.39.2.01 - Triidotironina
29.39.3.03 - Dehidorcortisona (prednisona)
29.39.3.04 - Acetônido de fluoxinolona
29.39.3.99 - Hemisuccinat de hidrocortisona
29.39.3.99 - Acetato de cloroprednisona
29.39.3.99 - Acetato de esoxicorticosterona U.S.P. (DOCA)
29.39.3.99 - Acetato de parametasona
29.39.3.99 - Cortisona
29.39.3.99 - Desoxicorticosterona
29.39.3.99 - Acetato de acetonido de fluoxinolona
29.39.3.99 - Flurandrenolona
29.39.3.99 - Decanoato de norandrostenolona
29.39.3.99 - Flumetasona
29.39.4.01 - Estrona (foliculina)
29.39.4.02 - Estriol
29.39.4.03 - Estradiol
29.39.4.04 - Progesterona U.S.P.
29.39.4.04 - Alfa e beta progesterona
29.39.4.05 - 17-alfa-etiniltestosterona
29.39.4.99 - Etinil-dehidoresterona
29.39.4.99 - Estirona (eftiniltestosterona) U.S.P.
29.39.4.99 - Estinil de enovid (17-alfa etinil 1,4 dehidroestradiol, 3 metil éter)
29.39.4.99 - Etinil estradiol 3-metil éter
29.39.4.99 - Etimilestradiol
29.39.4.99 - Valerianato de estradiol, Ciclopentenilpropionato de estradiol
29.39.4.99 - Acetato de 17-alfa-hidroxiprogesterona
29.39.4.99 - Mestranol
29.39.4.99 - Enantato de noretindrona
29.39.4.99 - Oxina de acetato de pregnadienolona
29.39.4.99 - Noretindrona
29.39.4.99 - 9 alfa, 11 beta-dicloro-6 alfa-fluoro-16 alfa, 17 alfa, 21-trihidroxipregna, 4-dion-3, 20-dion-16, 17-acetónido (fluclorolon)
29.39.4.99 - 9 alfa, 11beta-dicloro-6 alfa, 21-difluoro-16 alfa, 17 alfa-dihidroxipregna-1, 4-dion-320-16, 17-acetónido
29.39.4.99 - 6 beta-fluor-6 alfa, 7 alfa-di-fluorometilen-17 alfa-hidorxipregna-1, 4-dion-3,20-dion-17-acetato
29.39.4.99 - Acetato de noretindrona
29.39.4.99 - Delta 5.10.19 norandrosten-3-17-diona
29.39.4.99 - Benzoato de estradiol U.S.P.
29.39.4.99 - Capreato de 17-alfa-hidroxiprogesterona e metoxietinil estradiol
29.39.4.99 - Diacetato de etinodiol (diacetato do 17-alfa-etinil-4-estrona-s-beta-17-beta-diol)
29.39.4.99 - 17-alfa-acetoxi-9-alfa-fluoro-11 beta-hidroxi-pregn-4-en 3,20-ciona (acetato de flurogestona)
29.39.4.99 - Estrona-3 metil éter (1, 3, 5-estratien-17-ona-3-metil-eter) C19 H24 O2
29.39.4.99 - Acetato de clormadinona
29.39.4.99 - Acetato de estenobolona
29.39.4.99 - Equilina (3-hidroxiestral-1, 3, 5, 10)-7-tetaen-17-ona)
29.39.4.99 - Equilenina (3-hidroxiestral-1, 3, 5, 10)-6, 8-pentaen-17-ona
29.39.5.01 - Testosterona
29.39.5.02 - Metiltestosterona
29.39.5.99 - Metiandrostenolona
29.39.5.99 - Fenalpropionato de testosterona
29.39.5.99 - Fenilpropionato de norandostenolona
29.39.5.99 - Acetato de testosterona
29.39.5.99 - Caproato de testosterona
29.39.5.99 - Ciclopentenil proprionato de testosterona
29.39.5.99 - Emantato de testosterona
29.39.5.99 - Propionato de testosterona
29.39.5.99 - Caproato de testosterona
29.39.5.99 - Androstadienediona
29.39.5.99 - Dromostanolona
29.39.5.99 - Oximetolona
29.39.5.99 - Propionato de dromostanolona
29.39.5.99 - Dehidrotestosterona
29.39.5.99 - 19-Nortestosterona
29.39.5.99 - Acetato de 17-alfa-etinil-19-nortestosterona
29.39.5.99 - Acetato de 2-metil-delta-1-androsten-17-beta-ol-3-ona
29.39.5.99 - Acetato de dehidroisoandrosterona
29.39.5.99 - Noretandrolona
29.39.5.99 - Clorotestosterona
29.39.5.99 - Acetato de 4-clorotestosterona
29.39.5.99 - 19-nor-17-alfa-metilestosterona
29.39.5.99 - 19-nor-17-alfa-vinil-testosterona
29.39.5.99 - Valerianato de testosterona
29.39.5.99 - Undecanoato de testosterona
29.39.9.01 - Insulina
29.39.9.99 - 17-alfa-acetoxiprogesterona
29.40.0.01 - Pepsina
29.40.0.02 - Pancreatina recoberta
29.40.0.99 - Cloreto de lisozima
29.40.0.99 - Tripsina
29.40.0.99 - Hialuronidase
29.40.0.99 - Quimotripsina
29.42.1.01 - Morfina
29.42.1.03 - Etilmorfina
29.42.1.05 - Codeina
29.42.1.08 - Papaverina
29.42.1.09 - Tebaina
29.42.1.10 - Narcotina
29.42.1.99 - Cloridrato de dihidroxicodeinona
29.42.1.99 - Bitartrato de dihidroxicodeinona
29.42.1.99 - Cloridrato de dihidromorfinona
29.42.1.99 - Bitartrato de dihidrocodeinona
29.42.1.99 - Cloridrato de dihidromorfinona
29.42.1.99 - Cloridrato de hidroxi-dihidro-morfinona
29.42.2.01 - Quinina
29.42.2.03 - Cinchonina
29.42.9.04 - Pilocarpina
29.42.9.06 - Atropina
29.42.9.09 - Escopelamina
29.42.9.13 - Cafeina
29.42.9.18 - Estricnina
29.42.9.21 - Piperina
29.42.9.22 - Conina
29.42.9.99 - Nitrato de pilocarpina
29.42.9.99 - Cloridrato de pilocarpina
29.42.9.99 - Cloridrato de emetina
29.42.9.99 - Citrato de cafeína
29.42.9.99 - Tomatina
29.42.9.99 - Sulfato de vincaleucoblastina
29.42.9.99 - 8-Clorotoefilinato de 2-(Benzhidroloxi)-N-N-dimetiletilamina (dimenidrinato)
29.42.9.99 - 8-Cloroteofilina
29.43.0.99 - Glucose-1-fosfato
29.44.0.01 - Penicilinas
29.44.0.06 - Tirotricina
29.44.0.08 - Espiramicina (rovamicina)
29.44.0.99 - Monossuccinato ácido de clorafenicol
29.44.0.99 - Sulfato de tetraciclina
29.44.0.99 - Pristinamicina
29.44.0.99 - Cloridrato de metaciclina
29.44.0.99 - Cloridrato de oxitetraciclina
29.44.0.99 - Ftalato de eritromicina
29.44.0.99 - Cloridrato de doxiciclina
29.44.0.99 - Monosuccinato ácido de cloranfenicol
29.44.0.99 - Rifamicina B dietilamina
29.44.0.99 - Cloridrato de demeticlorotetraciclina
29.44.0.99 - Rifamicina S. V. sal sódico
29.45.0.99 - Isopropilato de alumínio
30.01.1.01 - Fígado dessecado, inclusive pulverizado, para uso opoterápico
30.01.1.02 - Hipófise dessecada, inclusive pulverizada, para uso opoterápico
30.01.1.99 - Os demais órgăos e glândulas dessecados, inclusive pulverizados, para uso opoterápico
30.01.2.01 - Extrato de fígado
30.01.2.02 - Extrato de bile
30.01.2.99 - Fator intrínseco, inclusive em pó, năo dosificado
30.01.2.99 - Concentrado hepático em pó, năo dosificado
30.01.2.99 - Pó pilórico, năo dosificado
30.01.2.99 - Extrato suparrenal, năo dosificado
30.01.2.99 - Extrato antropilórico, năo dosificado
30.01.2.99 - Extrato de baço, năo dosificado
30.01.2.99 - Fraçăo antitóxica do fígado, năo dosificado
30.01.2.99 - Extrato pancreático desproteinado estéril, em soluçăo
30.05.1.01 - Categute esterelizado
30.05.1.02 - Fio de seda esterelizado, para suturas cirúrgicas
30.05.1.03 - Fio de linho esterelizado, para suturas cirúrgicas
30.05.1.99 - As demais ligaduras esterelizadas, para suturas cirúrgicas
30.05.9.01 - Laminárias estéreis
35.04.1.99 - Peptona bacteriológica
38.19.0.21 - Reativos compostos para diagnósticos e laboratórios
39.06.1.99 - Heparina
39.06.1.99 - Polisacarídeo atóxico sucedâneo do plasma (dextrán)
95.08.0.01 - Cápsulas de gelatina vazias para medicamentos
(1) Classificaçăo provisória
Art. 2ş A ampliaçăo do setor industrial compreendido no art. 1ş somente poderá realizar-se com o cumprimento das formalidades correspondentes ŕ celebraçăo dos Ajustes de Complementaçăo, de conformidade com o estabelecido pela Resoluçăo 99 (IV).
CAPÍTULO II
Programa de Liberaçăo
Art. 3ş No anexo I do presente Protocolo figuram os gravames e demais restriçőes que vigerăo, em cada um dos países participantes, para a importaçăo dos produtos compreendidos no setor a que se refere o Capítulo I, sempre que sejam originários dos mesmos ou da Bolívia, do Equador ou do Paraguai.
Art. 4ş Os Governos dos países participantes reverăo anualmente suas respectivas concessőes no âmbito do presente Ajuste, visando uma paulatina reduçăo dos gravames do anexo I. Igual critério seguirăo em relaçăo aos gravames dos produtos que se incorporem ao mesmo, como consequęncia da ampliaçăo, prevista no Artigo 2ş, da lista respectiva.
Art. 5ş As negociaçőes a que se refere o Artigo anterior, e a consideraçăo e soluçăo dos demais assuntos vinculados ŕ marcha do presente Ajuste, levar-se-ăo a cabo, preferivelmente, durante os períodos de sessőes ordinárias da Conferęncia das Partes Contratantes, e ficarăo formalizadas através de Protocolos assinados por Plenipotenciários devidamente autorizados.
Art. 6ş Os Governos participantes do presente Ajuste realizarăo consultas prévias entre si, toda vez que se busque a inclusăo, em suas respectivas listas nacionais, de algum ou alguns dos produtos compreendidos no Artigo 1ş.
CAPÍTULO III
Qualificaçăo de Origem
Art. 7ş Os produtos compreendidos no programa de liberaçăo do presente Ajuste serăo considerados originários dos países participantes, ou da Bolívia, do Equador ou do Paraguai, quando tenham sido produzidos em seus territórios e cumpram com as disposiçőes sobre origem vigentes na ALALC.
Art. 8ş Os Governos participantes poderăo fixar requisitos específicos de origem para os produtos compreendidos no programa de liberaçăo do presente Ajuste, caso a Associaçăo já năo os tenha estabelecido.
Art. 9ş os requisitos específicos de origem que a Associaçăo fixa, com referęncia aos produtos objeto dęste Ajuste, prevalecerăo sobre os que se estabeleçam no anexo II do presente Protocolo.
Art. 10. Os requisitos de origem que se estabeleçam no presente Ajuste poderăo ser modificados visando, entre outros objetivos, a:
a) Adaptá-los ŕ evoluçăo da tecnologia; ou
b) Ajustá-los ŕ evoluçăo de novas condiçőes de produçăo na zona.
CAPÍTULO IV
Margens de preferęncia e medidas de harmonizaçăo
Art. 11. Os Governos participantes comprometem-se a preservar as margens de preferęncia para os produtos incluídos no programa de liberaçăo deste Ajuste, de conformidade com o disposto na Resoluçăo 53 (II) da Conferęncia ou nas normas que eventualmente a complementem ou substituam.
Art. 12. Os Governos dos países participantes procurarăo alcançar, através da execuçăo dos compromissos derivados do presente Ajuste, os objetivos a que se refere o artigo quinto, inciso a) da Resoluçăo 99 (IV).
CAPÍTULO V
Retirada de Concessőes
Art. 13. Qualquer país signatário ou aderente do presente Ajuste poderá retirar concessőes registradas no anexo I, através da outorga de adequada compensaçăo.
A solicitaçăo de retirada de concessőes deverá ser fundamentaa e comunicada aos Governos participantes através do Comitę Excutivo Permanente, com pelo menos sessenta dias de antecedęncia ŕ data da reuniăo, a que se refere o Artigo 5ş do presente Ajuste, na qual serăo celebradas as negociaçőes relativas ŕ retirada da concessăo.
CAPÍTULO VI
Adesăo
Art. 14. O presente Protocolo está aberto ŕ adesăo das Partes Contratantes năo signatárias do mesmo.
Os Governos dos países participantes do Ajuste e os das Partes Contratantes que solicitem adesăo ao mesmo, entabularăo as negociaçőes necessárias para determinar as obrigaçőes que corresponderăo a estas últimas.
CAPÍTULO VII
Denúncia do Ajuste
Art. 15. O Govęrno de qualquer dos países participantes poderá denunciar o presente Ajuste, transcorridos dois anos a partir da data de sua aplicaçăo por parte do mesmo.
Para ęsses efeitos, deverá comunicar sua decisăo aos demais Governos signatários e aderentes pelo menos trinta dias antes do depósito do respectivo instrumento de denúncia junto ao Comitę Executivo Permanente.
Formalizada a denúncia, os direitos e obrigaçőes contraídos pelo país denunciante cessarăo automaticamente, salvo no que se refere ŕs reduçőes de gravames e demais restriçőes recebidas e outorgadas até ęsse momento em cumprimento do programa de liberaçăo regulado pelo presente Ajuste, as quais continuarăo em vigor pelo prazo de um ano contado a partir da data de formalizaçăo da denúncia.
CAPÍTULO VIII
Disposiçőes Gerais
Art. 16. Os benefícios negociados no presente Ajuste entender-se-ăo automaticamente, sem a outorga de compensaçőes, ŕ Bolívia, ao Equador e ao Paraguai, independentemente de negociaçăo e adesăo ao mesmo.
Art. 17. O presente Ajuste entrará em vigor dentro do prazo de 60 (sessenta) dias após a data em que o Comitę Executivo Permanente lhe tenha declarado a compatibilidade com os princípios e objetivos do Tratado de Montevidéu, o prazo dentro do qual os Governos participantes se comprometem a adotar as providęncias que sejam necessárias para essa finalidade.
Art. 18. Para os efeitos dos artigos 5ş, 8ş e 10 do presente Ajuste, tanto a ampliaçăo das concessőes como o estabelecimento e revisăo dos requisitos específicos de origem figurarăo em Protocolos adicionais ao presente .
Art. 19. Os Governos participantes informarăo o Comitę Executivo Permanente sobre a marcha do presente Ajuste.
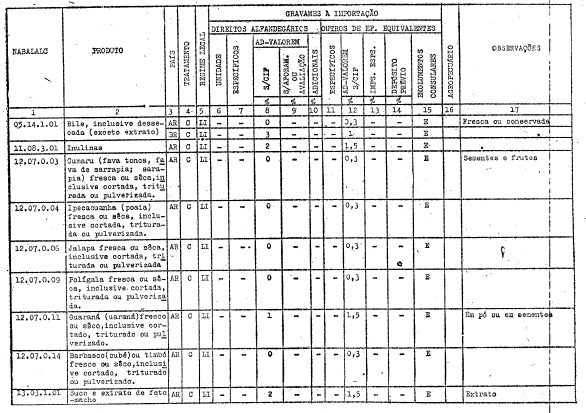
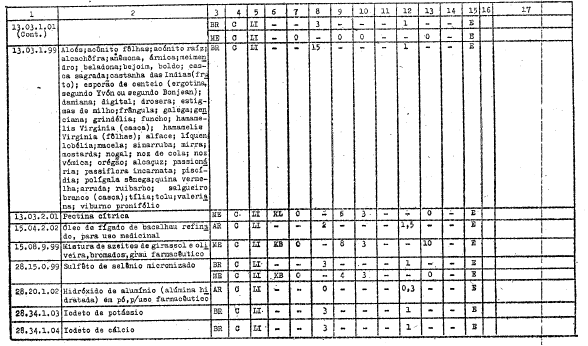
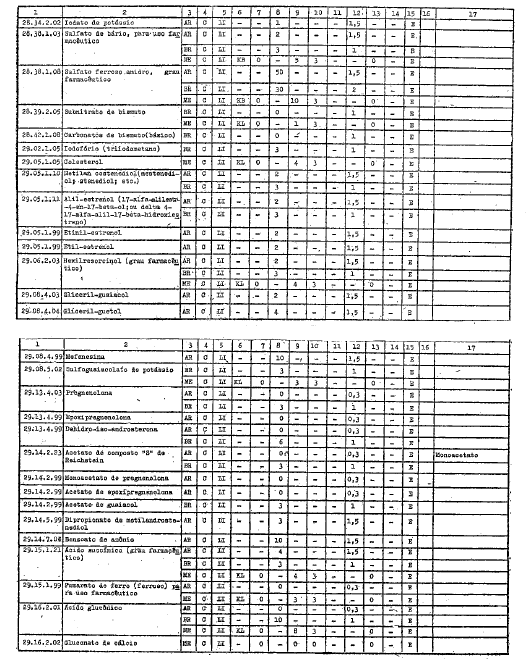
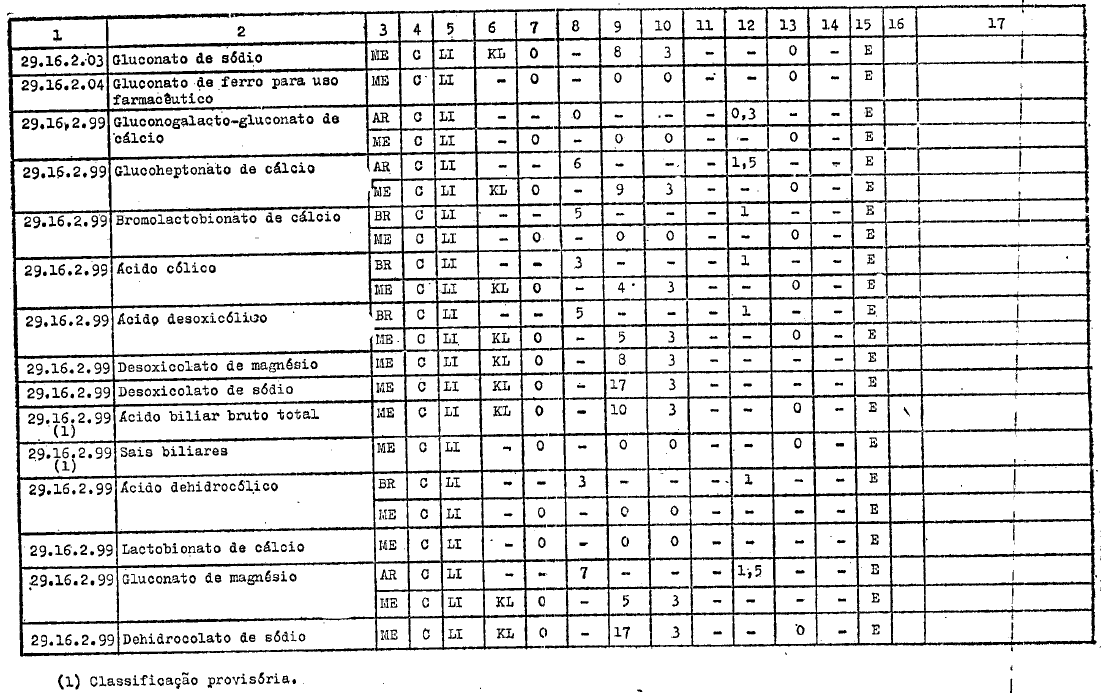
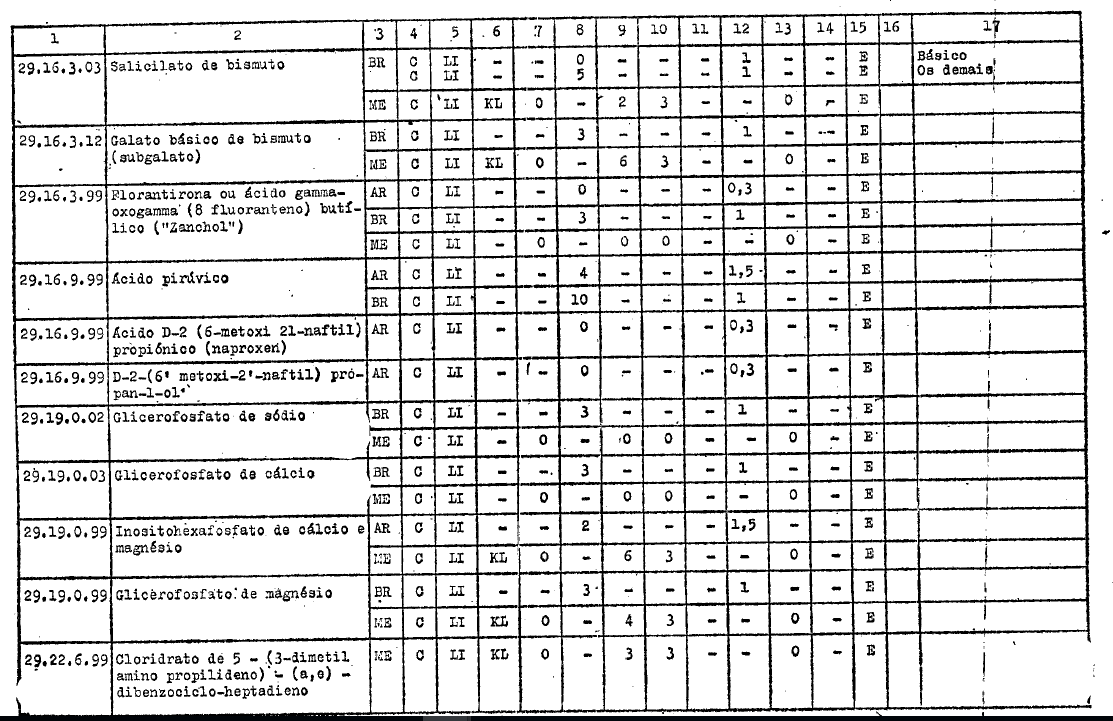
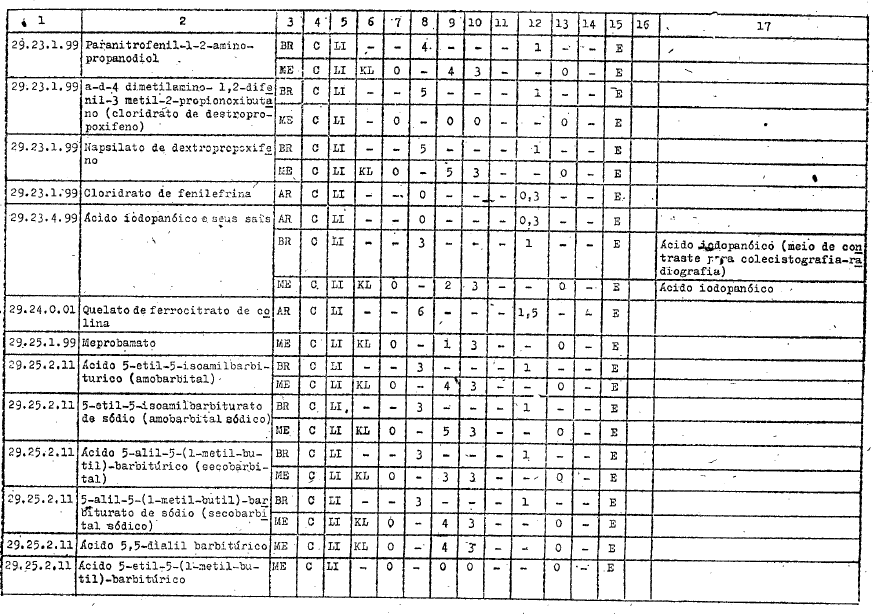
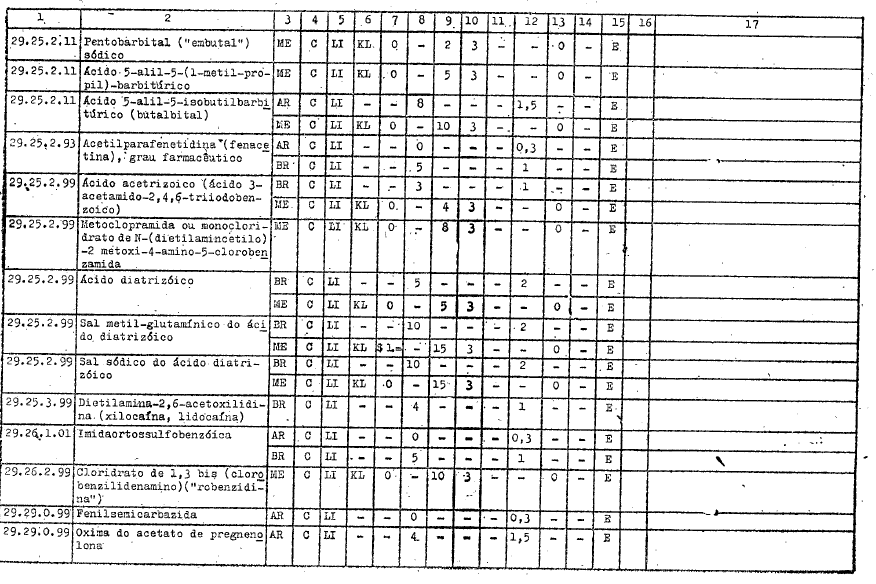
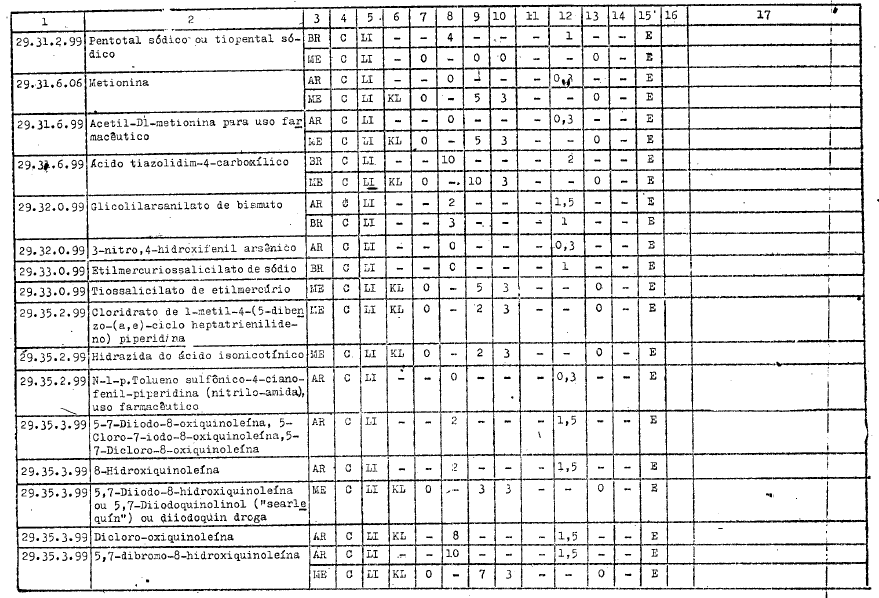
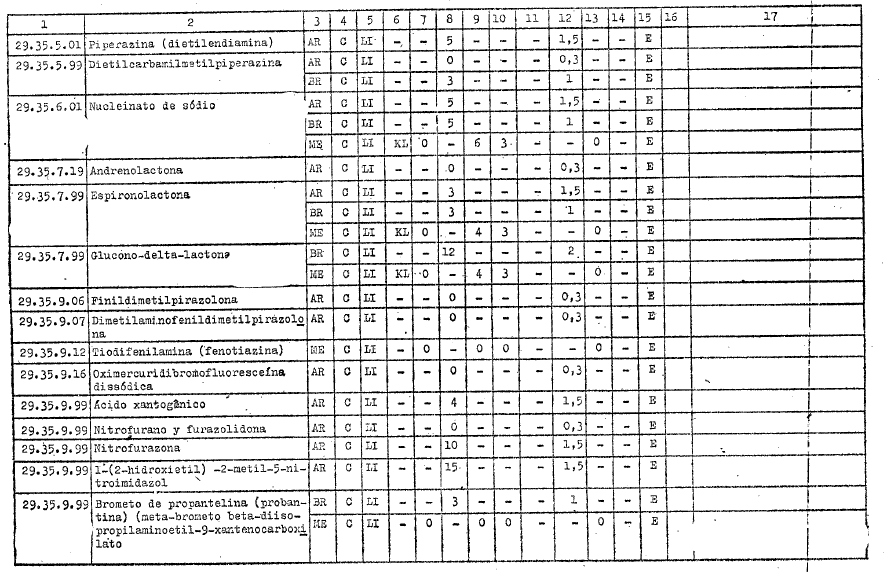
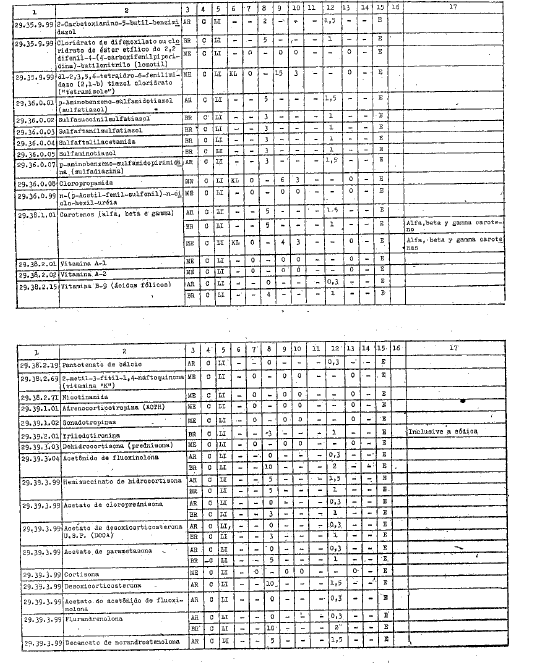
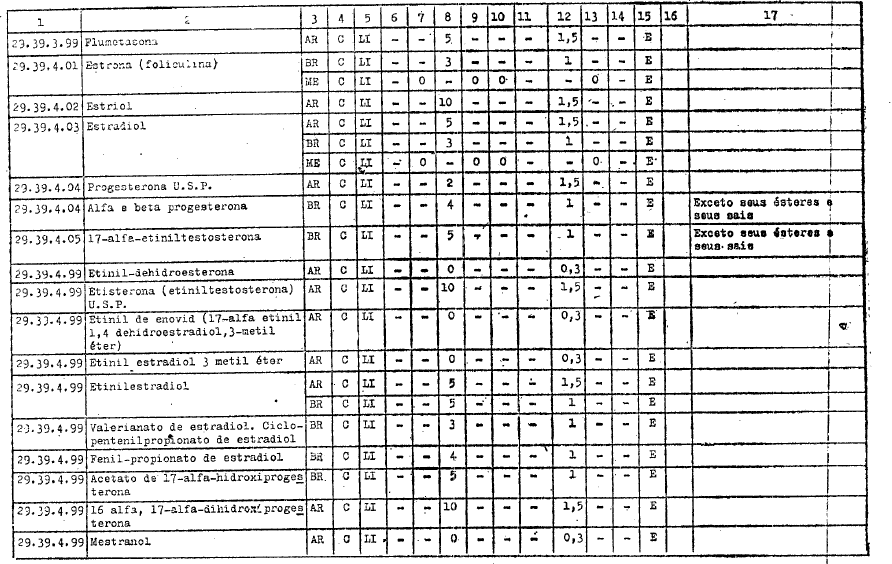
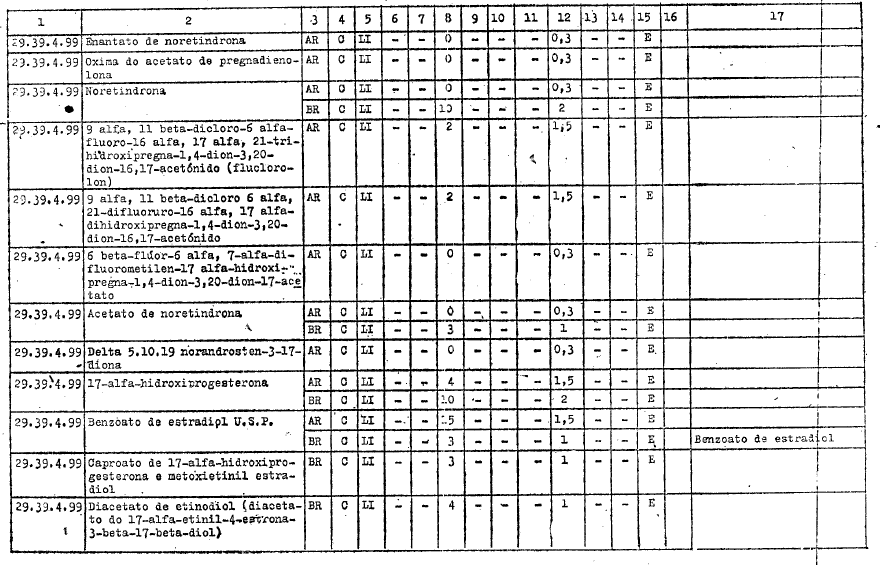
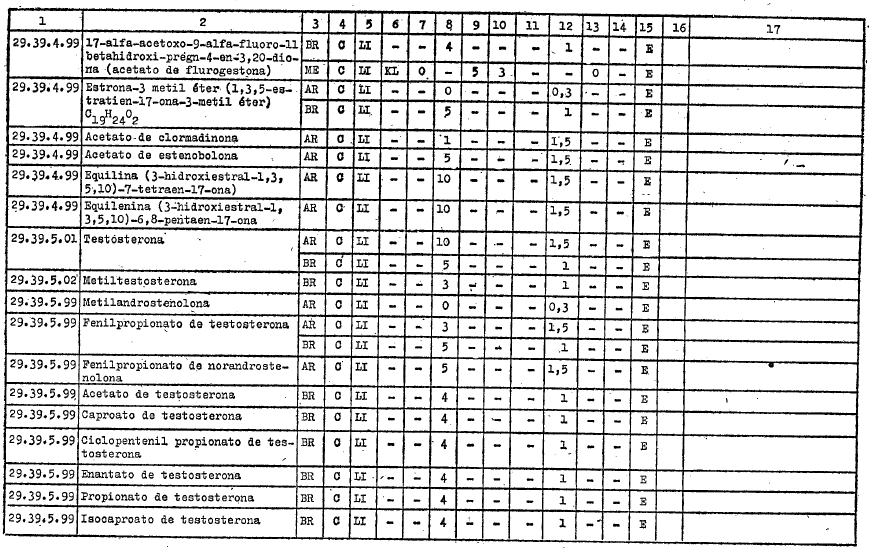
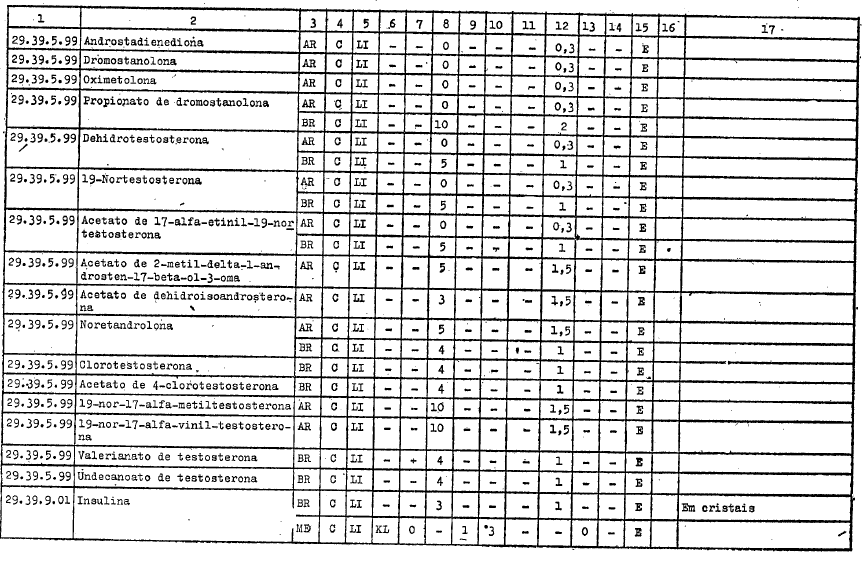
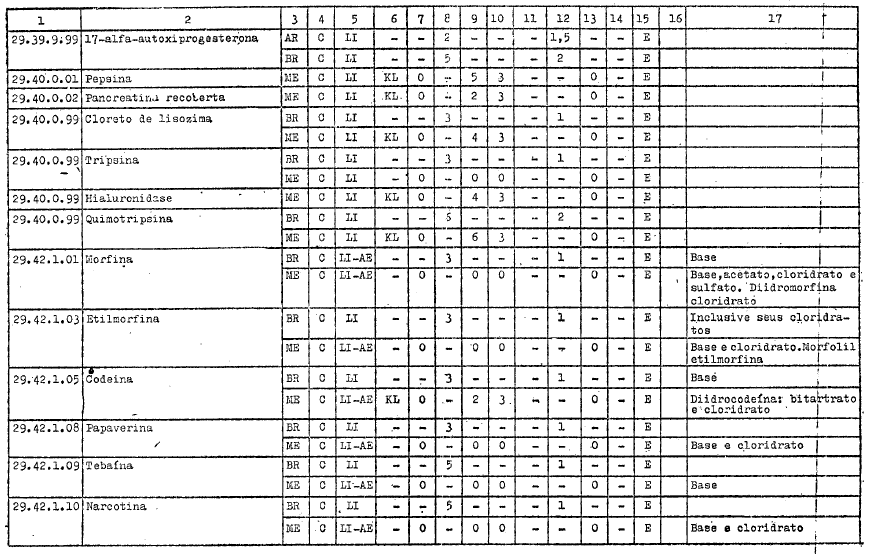
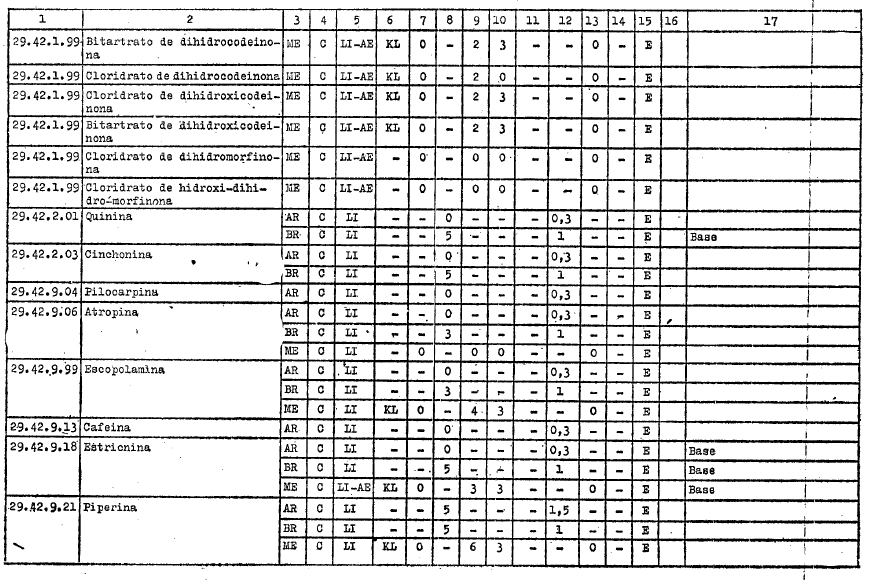
ANEXO I
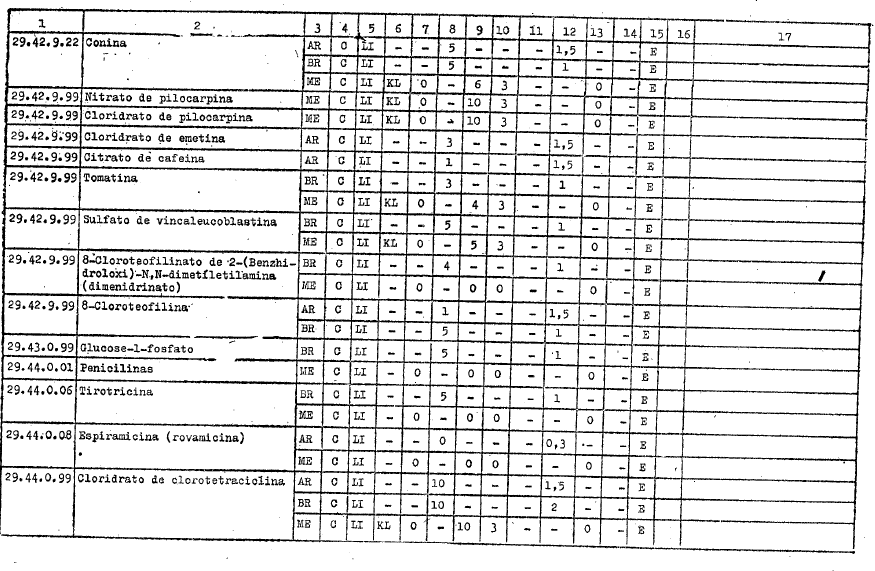
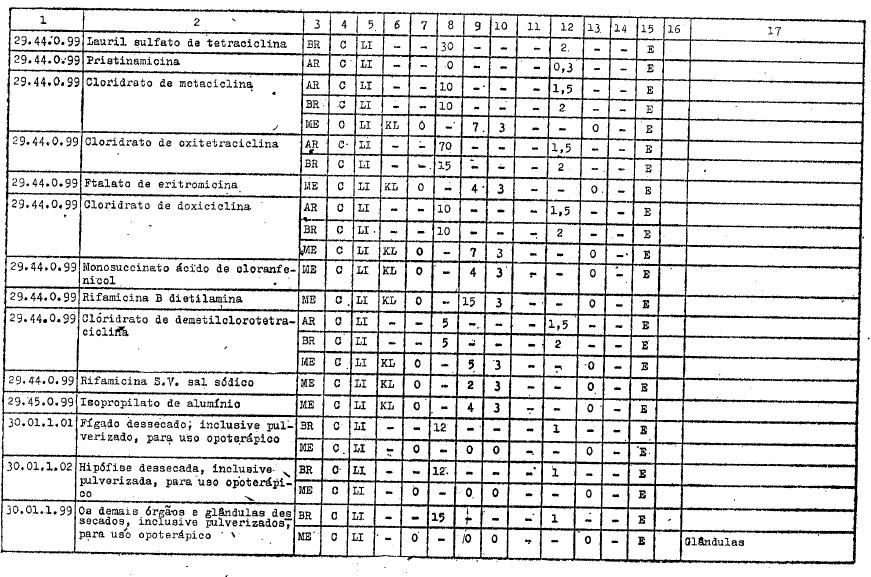
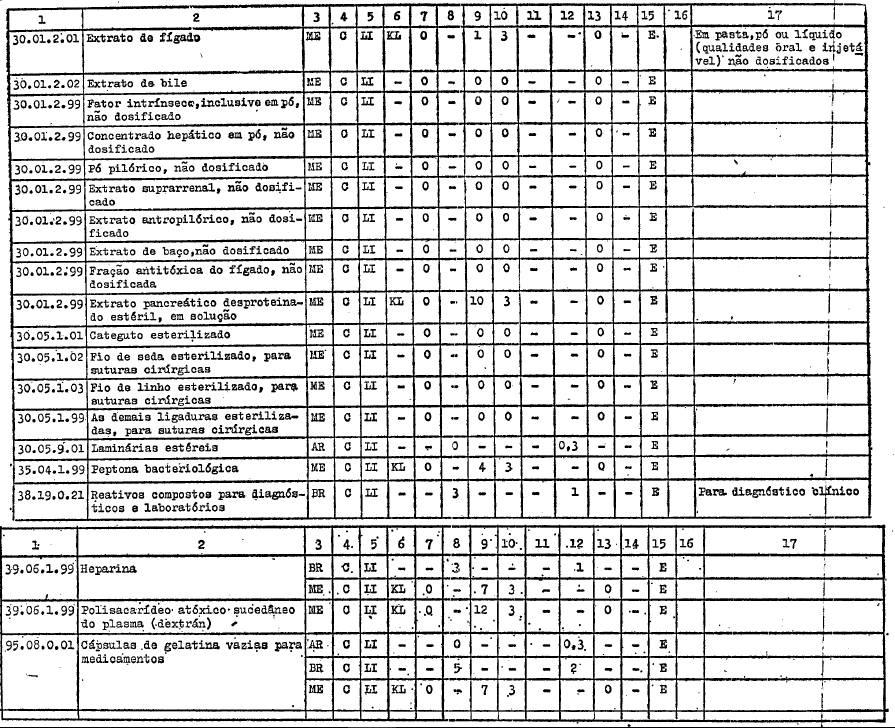
DIREITOS ALFANDEGÁRIOS, GRAVAMES DE EFEITOS EQUIVALENTES E RESTRIÇŐES APLICÁVEIS PELOS GOVERNOS PARTICIPANTES A IMPORTAÇĂO DOS PRODUTOS INCLUÍDOS NO ARTIGO 1ş DO PRESENTE AJUSTE
REFERĘNCIAS
C - Tratamento vigente no Ajuste
LI - Livre importaçăo
AE - Autorizaçăo especial
KL - Quilograma legal
KB - Quilograma bruto
E - Exigível
Em Fé Do Que, os respectivos Plenipotenciários assinam o presente Protocolo, feito na cidade de Montevidéu, aos quatro dias do męs de dezembro de mil novecentos e setenta, nos idiomas espanhol e portuguęs, sendo ambos os textos igualmente válidos.
A Secretaria do Comitę Executivo Permanente da Associaçăo Latino-Americana de Livre Comércio será a depositária do presente Protocolo, do qual enviará cópias devidamente autenticadas aos Governos participantes.
Pelo Governo da República Argentina Carlos S. Vailati.
Pelo Governo da República Federativa do Brasil Maury Gurgel Valente.
Pelo Governo dos Estados Unidos Mexicanos Mario Espinosa de los Reyes.